Longtemps considérés comme des débris cellulaires sans fonction biologique, les exosomes, et plus généralement les vésicules extracellulaires (VEs) sont aujourd’hui reconnues comme des vecteurs de matériel biologique ayant un rôle dans la communication intercellulaire. Le développement des connaissances sur le sujet a permis de mettre en évidence leur rôle dans certaines pathologies, mais aussi de dévoiler leur potentiel en tant que biomarqueur et outil thérapeutique.
Définition et biogenèse
Les vésicules extracellulaires (VEs) sont des vésicules de tailles et d’origines diverses sécrétées par les cellules eucaryotes dans le milieu extracellulaire. Ces vésicules transportent un cargo constitué de lipides, d’acides nucléiques et de protéines, en particulier les protéines associées à la membrane plasmique, au cytosol et celles impliquées dans le métabolisme des lipides.
Elles ont reçu au fil du temps et des recherches de nombreuses dénominations, et de nombreux sous-types existent, mais la nomenclature la plus récente les classe en trois catégories principales : les exosomes, les microvésicules (MVs), et les corps apoptotiques. Ces trois catégories se distinguent notamment par leur mode de formation, lequel a également un impact sur leur profil protéique et sur leur taille :
- Les exosomes ont une taille de 30-150nm, et se forment via la voie endosomale: les vésicules exosomales se forment par bourgeonnement à l’intérieur de la membrane des endosomes précoces, qui se transforment alors en corps multivésiculaires (CMV). Les CMV matures vont ensuite soit suivre la voie lysosomale pour être dégradés, soit libérer leur contenu par exocytose à la membrane plasmique, les exosomes arrivant ainsi dans l’espace extracellulaire ;
- Les microvésicules ont des tailles très variables, comprises entre 100 nm – 1 μm, et se forment par bourgeonnement vers l’extérieur et pincement de la membrane plasmique, libérant les MVs nouvellement formées directement dans l’environnement extracellulaire ;
- Les corps apoptotiques sont libérés par les cellules mourantes dans l’espace extracellulaire. Leur diamètre varie de 50 nm à 5000 nm, la majorité étant plutôt grands. Ces corps se forment par la séparation de la membrane plasmique du cytosquelette en raison de l’augmentation de la pression hydrostatique après la contraction de la cellule.
La suite de l’article se concentrera sur les vésicules extracellulaires produites par les cellules non apoptotiques, soit les exosomes et les EVs. Souvent, par abus de langage, « vésicules extracellulaires » désigne toutes les vésicules qui ne sont pas des exosomes (microvésicules et autres sous-types).
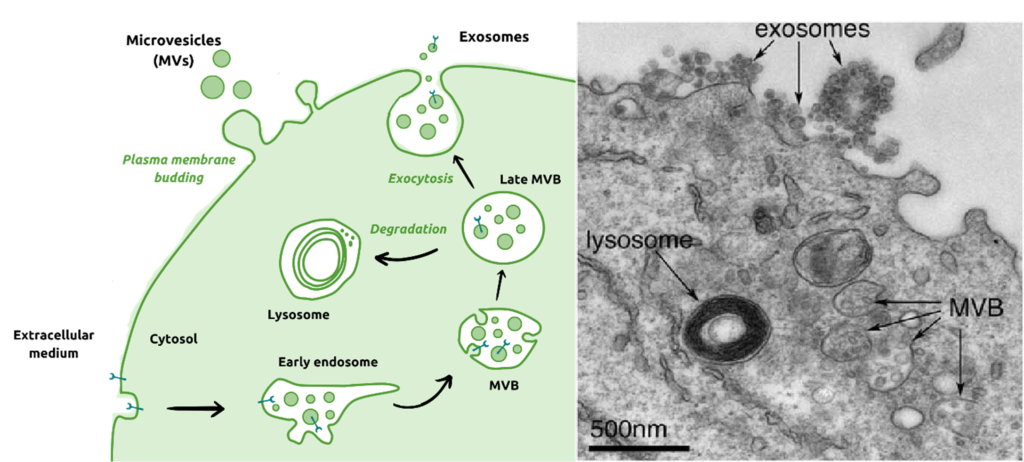
Biogenèse des exosomes et microvésicules. Gauche - adapté de Kowal et al., 2014 ; droite – cellule cancéreuse sécrétant des exosomes, Edgar et al., 2016. MVB : multi-vesicular bodies
Des fonctions biologiques diverses et contexte-dépendantes
Pendant longtemps, les exosomes et les MVs étaient considérés comme un moyen pour les cellules d’éliminer des composants cellulaires excédentaires et/ou non fonctionnels. Depuis, de nombreuses recherches ont permis de mettre en évidence leur rôle dans de nombreux processus biologiques : la maintenance cellulaire (recyclage des protéines de la surface cellulaire et des molécules de signalisation), la communication cellule-cellule, l’angiogenèse, la présentation d’antigènes, la coagulation, l’homéostasie cellulaire, l’inflammation, etc.
C’est grâce à leur capacité à transporter et transférer des cargos actifs très divers et à les livrer à une autre cellule, voisine ou éloignée, que les vésicules extracellulaires sont capables de modifier les fonctions de la cellule réceptrice, et donc d’impacter de nombreux processus biologiques. D’ailleurs, des exosomes ont été isolés de divers liquides organiques, tels que le sang, la salive, le plasma, l’urine, le sperme, le liquide céphalorachidien, etc. La cellule « réceptrice » des exosomes va interagir avec ceux-ci par endocytose, fusion à la membrane, ou interaction ligand/récepteur, ce qui aboutira soit à l’internalisation de leur contenu, soit au déclenchement de cascades de signalisation par exemple.
Cet impact sur des processus biologiques est mis en jeu dans les cellules saines, mais également dans le contexte de nombreuses pathologies telles que le cancer, les maladies neurodégénératives, les infections ou les maladies auto-immunes.
Les applications médicales
Le potentiel des VEs et exosomes comme biomarqueurs
Les exosomes et VEs sont produits par les cellules, en conditions saines comme en conditions pathologiques. Ils contiennent des protéines, des lipides, des métabolites et des acides nucléiques qui reflètent l’état physiologique de leur cellule d’origine : cela en fait donc une source de biomarqueurs pour le diagnostic clinique. Dans la littérature, plusieurs biomarqueurs typiques de pathologies ont été isolés à partir d’exosomes : on peut citer par exemple pour la maladie de Parkinson, l’alpha synucléine qui a été isolée à partir d’exosomes plasmatiques. De plus, les VEs sont présentes dans de nombreux fluides corporels : elles peuvent donc être récoltées de manière non invasive par biopsie liquide.
En oncologie, le diagnostic via les marqueurs exosomaux pourrait permettre de détecter de manière précoce des altérations génétiques ou phénotypiques, notamment grâce aux acides nucléiques contenus dans les vésicules. Cette approche diagnostique a donc plusieurs avantages sur la méthode classique par biopsies tissulaires, qui est invasive et qui présente un biais en raison de l’hétérogénéité des tumeurs. Au-delà du diagnostic précoce, les exosomes présentent également un intérêt dans le cadre du développement des traitements personnalisés, pour les pronostics, et globalement pour le suivi de traitement.
Le potentiel des exosomes comme outils thérapeutiques
Deux approches sont principalement utilisées dans les produits actuellement en développement : l’utilisation des VEs en tant de vecteurs, pour la délivrance ciblée de médicaments, et l’utilisation de VEs purifiées dérivées de cellules, en tant que « principe actif ».
Les exosomes comme vecteurs
Dans cette approche, les exosomes peuvent être chargés de divers cargos thérapeutiques selon les besoins du traitement. Les exosomes peuvent être modifiés ou fonctionnalisés pour cibler spécifiquement certaines cellules ou tissus dans l’organisme, améliorant ainsi l’efficacité et la précision du traitement. En tant que « transporteurs naturels », les exosomes présentent des avantages considérables : ils ont une immunogénicité et une toxicité faibles, ils protègent leur cargo de la dégradation, et sont capables de traverser la membrane cytoplasmique et la barrière hémato-encéphalique. Cette approche pourrait donc permettre de réduire les effets secondaires indésirables, d’améliorer l’efficacité des traitements, ou encore d’atteindre des tissus spécifiques.
Les VEs dérivés de cellules comme thérapie
Avec cette stratégie, les VEs, souvent les exosomes, sont collectés à partir du milieu de culture de cellules spécifiques : souvent des cellules souches (mésenchymateuses, neurales, etc.) mais aussi des cellules cancéreuses, des plaquettes, des cellules immunitaires, etc.
Les exosomes dérivés de cellules peuvent être utilisés comme produits thérapeutiques en tant que tel, sans ajout de cargo spécifique. En effet, les exosomes « héritent » d’effets thérapeutiques similaires à ceux de leurs cellules parentales : les exosomes dérivés de cellules souches mésenchymateuses ont par exemple un potentiel important en médecine régénérative. Cette alternative « cell-free » aux traitements par cellules souches pourrait présenter plusieurs avantages, tels qu’une immunogénicité et une toxicité moindres, un accès facilité, une meilleure conservation, et l’absence de potentiel tumorigène.
Les thérapies exosomales, ou l’utilisation des exosomes comme vecteurs, sont des approches largement investiguées en oncologie, avec de nombreux projets en développement pour le traitement de cancers.
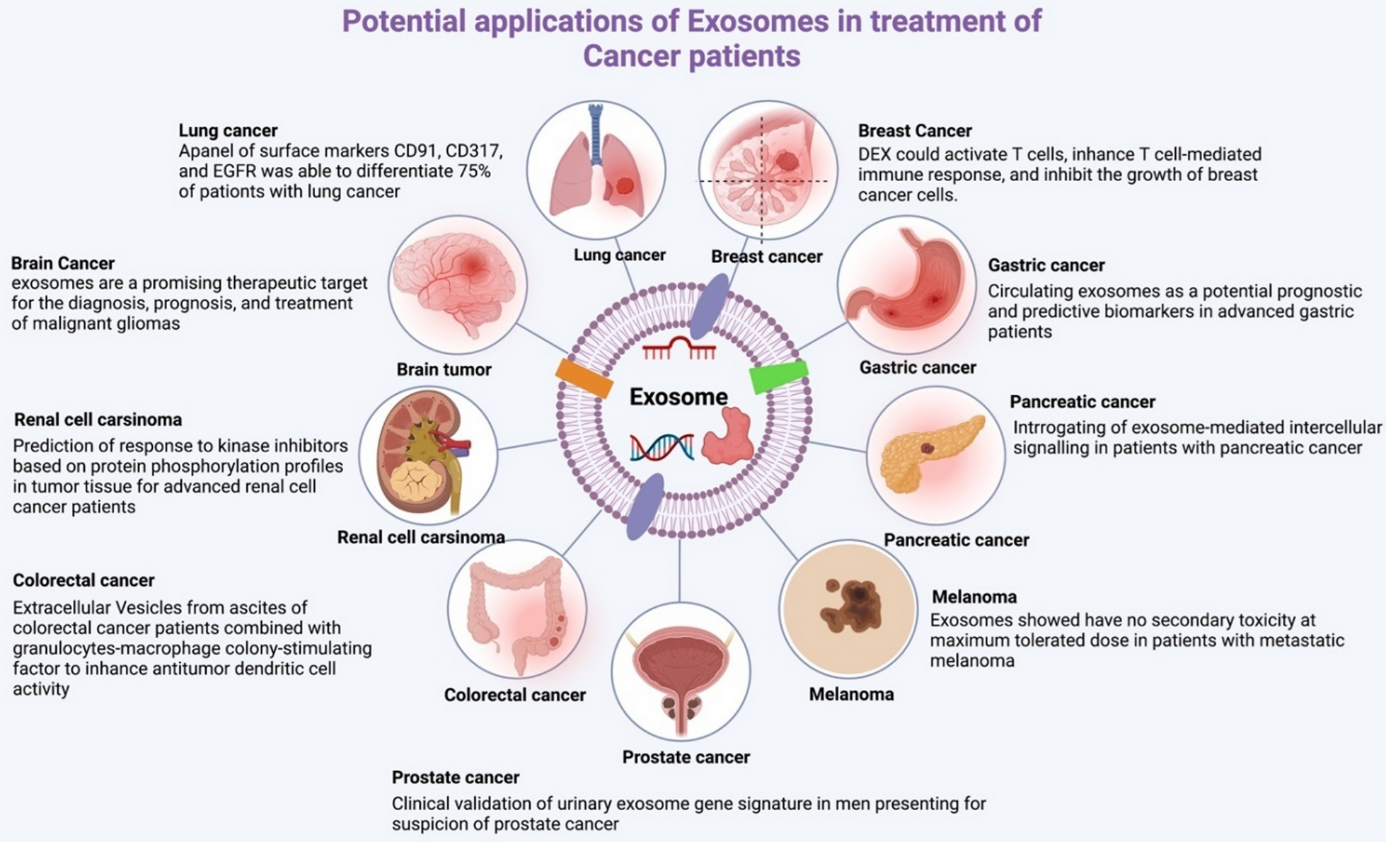
Applications potentielles des exosomes dans le cancer ; Hussen, B.M et al., 2022
Défis
Malgré la densité des recherches sur les vésicules extracellulaires et les exosomes, et la croissance rapide du secteur, plusieurs défis, notamment techniques, demeurent à relever.
Purification et caractérisation
Les techniques d’isolement et de purification sont encore suboptimales et peu standardisées. L’isolement des exosomes est difficile car certains composants des fluides biologiques tels que les lipoprotéines ou d’autres VEs ont des tailles qui se chevauchent avec celles des exosomes (30-150 nm).
A ces difficultés s’ajoutent la complexité de caractérisation : l’analyse approfondie des caractéristiques des VEs est souvent rendue difficile par l’hétérogénéité des isolats, qui se traduit par une distribution mixte des tailles, et des difficultés à établir le profil du contenu des vésicules.
De ces problématiques découlent les questions de bioproduction des exosomes, en termes de reproductibilité, de sûreté et de coût. Des lignes directrices et des standards doivent être définis dans le respect des règlementations liées aux produits biopharmaceutiques, afin d’aboutir à une utilisation des exosomes en clinique.
Délivrance, dosage et pharmacocinétique
Un défi important pour le développement futur des VEs est le contrôle de leur adressage vers les sites cibles et le maintien de leur efficacité. Pour atteindre cet objectif, plusieurs questions se posent : la fréquence de traitement nécessaire pour maintenir leur effet (dosage, demi-vie des exosomes dans les tissus, etc.) et les effets secondaires des traitements, en particulier à long terme. Une meilleure connaissance de la biologie des VEs et des exosomes, notamment des mécanismes d’encapsulation du cargo, est nécessaire pour optimiser ces étapes.
Analyse du marché des exosomes et vésicules extracellulaires
Pipeline
Le développement du champ des exosomes et des vésicules intracellulaires étant relativement récent, il n’y a actuellement aucun produit sur le marché. Néanmoins, étant donné les perspectives prometteuses comme outil de diagnostic, outil thérapeutique ou plateforme technologique, l’enthousiasme autour de ces approches est important, ce qui se traduit par un pipeline mondial riche avec 420 produits uniques en développement.
La majorité des produits dans le pipeline sont des exosomes (59%), ou des vésicules extracellulaires (23%). Ces dernières désignent, par abus de langage, toutes les vésicules d’origine eucaryote qui ne sont pas des exosomes. On peut également noter que les vésicules d’origine microbienne, type outer-membrane vesicles (OMVs) de bactéries ou virus-like-vesicles (VLV) de virus, représentent également une part importante du pipeline (17%). Ces projets ont été retirés du reste de l’analyse pour se concentrer sur l’analyse du pipeline des exosomes et vésicules intracellulaires, soit 347 produits uniques.
Pipeline par type
Pipeline par phase*
*produits en développement hors OMVs et VLVs
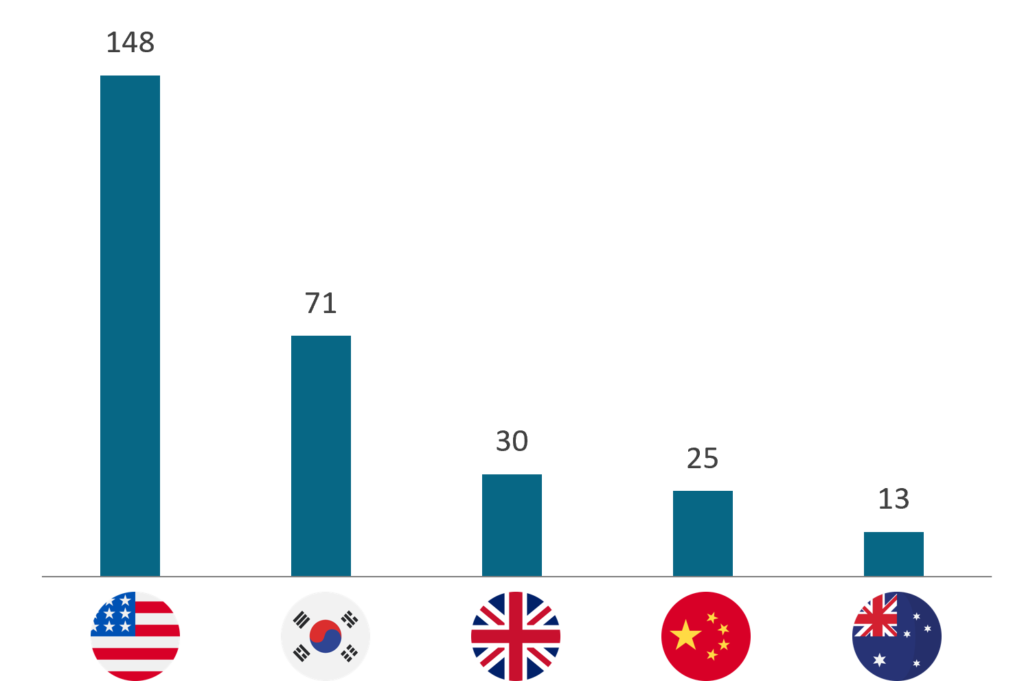
Les projets dans le pipeline sont principalement dans des phases précoces (discovery ou préclinique), avec seulement 11% de projets en phase clinique. Le pipeline étant assez riche, cela correspond tout de même à 40 projets impliquant des EVs ou exosomes actuellement en essais cliniques. Les cinq pays comptant le plus de produits en développement sont les USA, la Corée du Sud, le Royaume-Uni, la Chine et l’Australie. Les Etats-Unis et la Corée du Sud sont loin devant, totalisant à eux deux 219 produits uniques en développement, soit 63% du pipeline.
Pipeline par pays
Pipeline par aire thérapeutique
En termes d’aires thérapeutiques, les applications sont assez variées, comme illustré par le top 10 par nombre de produits en développement. A noter que les trois premières indications ciblées sont l’oncologie, la neurologie, et les maladies infectieuses.
Parmi les projets les plus avancés, on peut citer ExoFlo™, développé par Direct Biologics. C’est un produit contenant des facteurs de croissance et des vésicules extracellulaires, notamment des exosomes, isolés à partir de cellules souches mésenchymateuses. Le candidat est actuellement en essais cliniques de phase III notamment pour le traitement du syndrome de détresse respiratoire aiguë modéré à sévère, les séquelles post-aiguës du COVID-19, le rejet de greffe, ou encore la maladie de Crohn réfractaire. Diasome pharmaceuticals a également commencé un essai clinique de phase III pour sa technologie de vésicules ciblant les hépatocytes (HDV platform), ayant pour but la délivrance ciblée de l’insuline dans le traitement du diabète de type 2.
Tendances & acteurs principaux
Le marché des exosomes est encore très récent, et croît d’année en année avec des produits en développement, notamment clinique. Cette tendance à la hausse s’illustre notamment par le nombre d’essais cliniques en cours portant le tag « exosomal therapy », qui est globalement en hausse depuis 2017.
L’engouement autour des exosomes et des VEs se traduit également sur le marché par la pluralité des acteurs, ainsi que par des deals importants. On peut citer par exemple les deals conclus en 2020 par Evox Therapeutics, d’abord avec Takeda pour un partenariat centré sur les maladies rares d’une valeur de plus de 800 M$, puis un partenariat de plus d’un milliard de dollars avec Eli Lilly, pour le traitement de maladies neurologiques. Les deux deals concernent le développement de thérapies utilisant la plateforme technologique basée sur les exosomes d’Evox Therapeutics.
A noter également de nombreuses levées de fonds pour des biotechs développant des exosomes. On peut citer tout récemment EXO Biologics, qui a levé 16 M$ pour poursuivre le développement de thérapies basées sur des vésicules extracellulaires dérivées de cellules souches mésenchymateuses.
Essais cliniques*
*taggués « exosomal therapy »
Acteurs

Conclusion
Les exosomes représentent une modalité innovante et prometteuse dans le domaine de la médecine régénérative et du diagnostic. Leur capacité à agir comme des vecteurs thérapeutiques naturels, leur potentiel dans le diagnostic précoce des maladies et leur rôle dans la régulation des processus biologiques offrent de vastes opportunités pour des applications médicales. L’effort de recherche continu a permis d’amener des projets au stade clinique, et continue à aboutir à des innovations techniques et médicales qui ont le potentiel d’améliorer le traitement et la prise en charge de nombreuses pathologies.

Cet article est un extrait de notre Immunowatch « Exosomes & Other Extracellular vesicles » publiée en Juillet 2024. Vous pouvez la télécharger en intégralité sur le lien ci -dessous :
Immunowatch – Edition 9 – Exosomes & Other Extracellular Vesicles
Nos autres watchs sont disponibles sur la page dédiée :
Si vous cherchez du soutien dans vos projets en lien avec les exosomes et les vésicules extracellulaires, n’hésitez pas à explorer notre offre de services, et à nous contacter pour échanger.
Nous serons ravis de mettre à profit notre expertise pour vous aider à atteindre vos objectifs !
Sources
- GlobalData Avril 2024
- Di Bella, M. A. (2022). Overview and Update on Extracellular Vesicles : Considerations on Exosomes and Their Application in Modern Medicine. Biology, 11(6), 804. https://doi.org/10.3390/biology11060804
- Doyle, L. M., & Wang, M. Z. (2019). Overview of Extracellular Vesicles, Their Origin, Composition, Purpose, and Methods for Exosome Isolation and Analysis. Cells, 8(7), 727. https://doi.org/10.3390/cells8070727
- Edgar, J. R. (2016). Q&A : What are exosomes, exactly? BMC Biology, 14(1), 46. https://doi.org/10.1186/s12915-016-0268-z
- Gao, M., Gao, W., Papadimitriou, J. M., Zhang, C., Gao, J., & Zheng, M. (2018). Exosomes—The enigmatic regulators of bone homeostasis. Bone Research, 6(1), 1‑13. https://doi.org/10.1038/s41413-018-0039-2
- Hussen, B. M., Faraj, G. S. H., Rasul, M. F., Hidayat, H. J., Salihi, A., Baniahmad, A., Taheri, M., & Ghafouri-Frad, S. (2022). Strategies to overcome the main challenges of the use of exosomes as drug carrier for cancer therapy. Cancer Cell International, 22(1), 323. https://doi.org/10.1186/s12935-022-02743-3
- Kowal, J., Tkach, M., & Théry, C. (2014). Biogenesis and secretion of exosomes. Current Opinion in Cell Biology, 29, 116‑125. https://doi.org/10.1016/j.ceb.2014.05.004
- Mosquera-Heredia, M. I., Morales, L. C., Vidal, O. M., Barceló, E., Silvera-Redondo, C., Vélez, J. I., & Garavito-Galofre, P. (2021). Exosomes : Potential Disease Biomarkers and New Therapeutic Targets. Biomedicines, 9(8), 1061. https://doi.org/10.3390/biomedicines9081061
- Muthu, S., Bapat, A., Jain, R., Jeyaraman, N., & Jeyaraman, M. (2021). Exosomal therapy—A new frontier in regenerative medicine. Stem Cell Investigation, 8, 7. https://doi.org/10.21037/sci-2020-037
- Tan, F., Li, X., Wang, Z., Li, J., Shahzad, K., & Zheng, J. (2024). Clinical applications of stem cell-derived exosomes. Signal Transduction and Targeted Therapy, 9(1), 1‑31. https://doi.org/10.1038/s41392-023-01704-0
- Wang, X., Tian, L., Lu, J., & Ng, I. O.-L. (2022). Exosomes and cancer—Diagnostic and prognostic biomarkers and therapeutic vehicle. Oncogenesis, 11(1), 1‑12. https://doi.org/10.1038/s41389-022-00431-5
- https://www.labiotech.eu/trends-news/evox-therapeutics-eli-lilly/
- https://bioinformant.com/exosomes